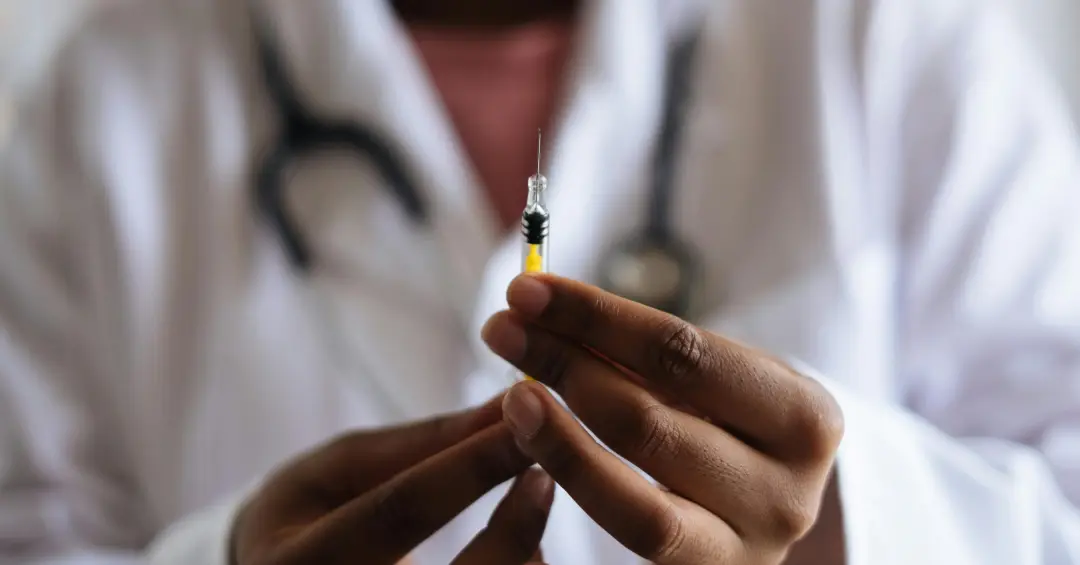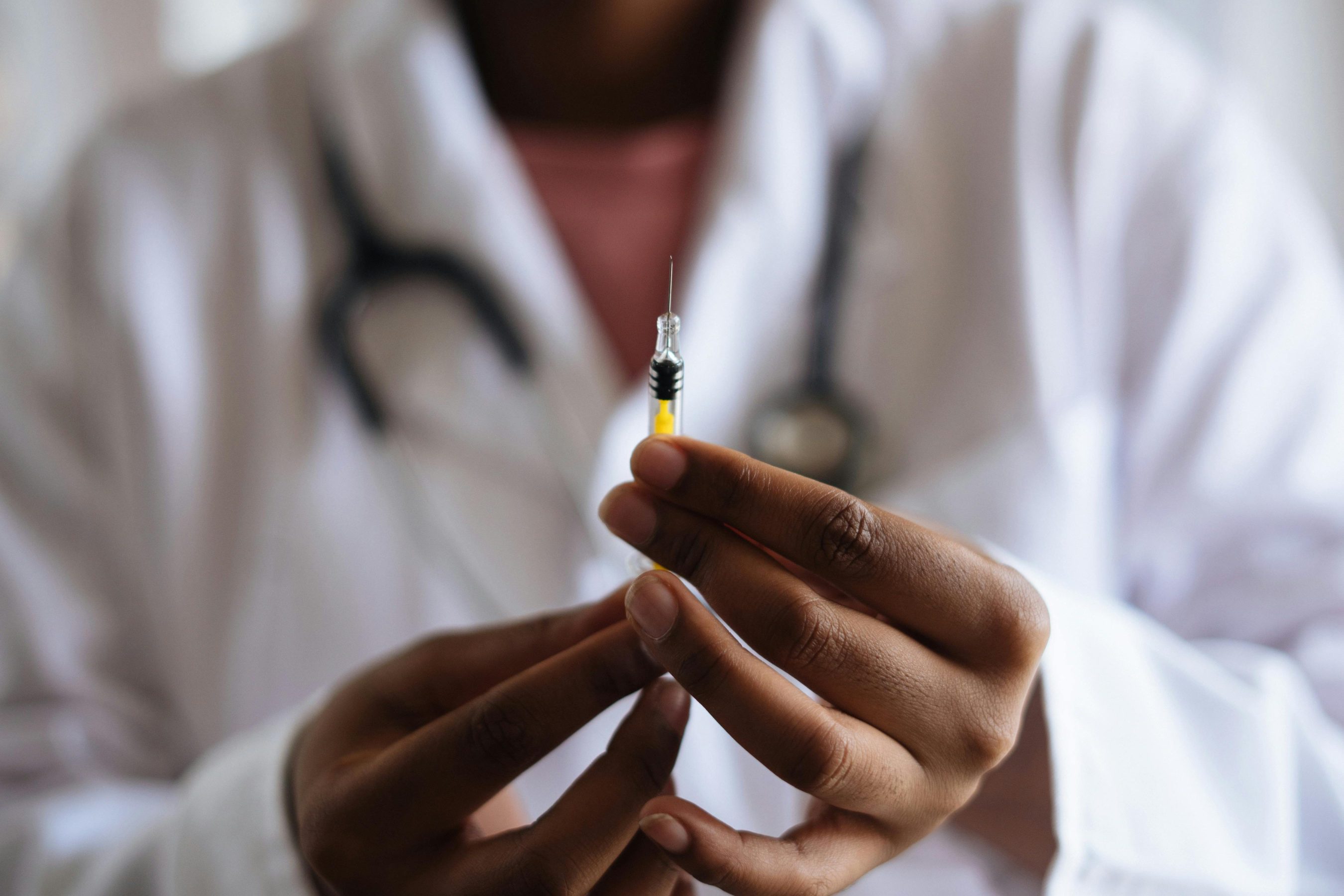
A Agência Nacional de Vigilância Sanitária (Anvisa) colocou em debate uma minuta de norma — ainda não aprovada e sujeita à votação — para endurecer o controle sobre versões manipuladas das chamadas “canetas” usadas no tratamento da obesidade e do diabetes tipo 2.
Na prática, a proposta não proíbe a manipulação, mas cria exigências que visam tornar o processo pouco mais controlado. Ainda assim, há ponderações por parte de especialistas.
Uma das principais mudanças está na entrada dos insumos – ou seja, das substâncias usadas para produzir esses medicamentos, como a tirzepatida e a semaglutida – no País. A proposta determina que todo lote desse tipo de ‘ingrediente’ deverá passar por avaliação prévia e por análise em laboratório no Brasil antes de ser liberado.
O importador terá que apresentar um conjunto de documentos técnicos ao Instituto Nacional de Controle de Qualidade em Saúde (INCQS), com informações sobre como o produto foi fabricado, sua composição e os testes realizados.
Mesmo após a chegada ao País, a carga ficará retida na alfândega até a conclusão dos testes laboratoriais. A liberação só acontece com um laudo técnico favorável.
Outro ponto é que o controle será feito por lote, mas o texto não detalha completamente se será necessário repetir todo o processo a cada nova importação de um mesmo lote.
Testes de qualidade passam a ser obrigatórios
A Anvisa também define quais testes precisam ser feitos tanto na substância usada na fabricação quanto no produto final manipulado.
Entre eles estão análises para verificar a pureza, a composição, a presença de impurezas e a segurança do produto, incluindo testes de esterilidade. A norma também estabelece limites para impurezas.
Farmácias passam a monitorar efeitos adversos
Outra mudança é a exigência de que farmácias acompanhem a segurança dos produtos que manipulam.
Elas terão que registrar possíveis efeitos colaterais relatados por pacientes e manter um banco de dados com essas informações.
Casos mais graves deverão ser comunicados à Anvisa em até 15 dias, e situações consideradas urgentes, em até 72 horas. Os dados deverão ser armazenados por até 20 anos.
O texto também reforça que esses medicamentos só podem ser manipulados com receita médica para um paciente específico, antes do preparo. Ou seja, farmácias não poderão produzir esse tipo de produto antecipadamente para manter em estoque.
Norma é considerada insuficiente
Apesar do avanço, especialistas avaliam que esse conjunto de testes ainda pode não ser suficiente para garantir a eficácia e a segurança desses medicamentos.
Outro ponto que chama atenção é que a proposta não menciona o Certificado de Adequação da Documentação do Insumo Farmacêutico Ativo (CADIFA), um instrumento que vinha sendo importante para garantir a qualidade e a rastreabilidade das substâncias usadas na produção. Caso venha a ser excluído, especialistas acreditam se tratar de um retrocesso.
A Sociedade Brasileira de Endocrinologia e Metabologia (SBEM) também se posicionou sobre a norma. A entidade afirma que o texto não resolve os principais riscos associados ao uso das “canetas” manipuladas. Segundo a entidade, esses medicamentos são complexos e seu comportamento no organismo não pode ser totalmente previsto apenas por testes laboratoriais.
“Pequenas diferenças na produção ou na composição podem afetar a eficácia, a segurança e até gerar reações inesperadas”, afirma.
A SBEM também defende que, embora a Anvisa expresse que esse tipo de medicamento só deve ser manipulado de forma individualizada — e não em fabricação em escala, inclusive com estoques para venda —, a regra não vai direto ao ponto e não cria artifícios realmente eficazes para lidar com esse tipo de problema.
Diante disso, a SBEM defende a proibição da manipulação desses medicamentos como a forma mais assertiva de reduzir riscos.